Un karst est un massif calcaire dont le paysage est en grande partie formé par l’action de l’eau sur cette roche. Ce paysage montre des formes d’érosion de surface caractéristiques, mais aussi des formations souterraines (cavités et concrétions) spécifiques.
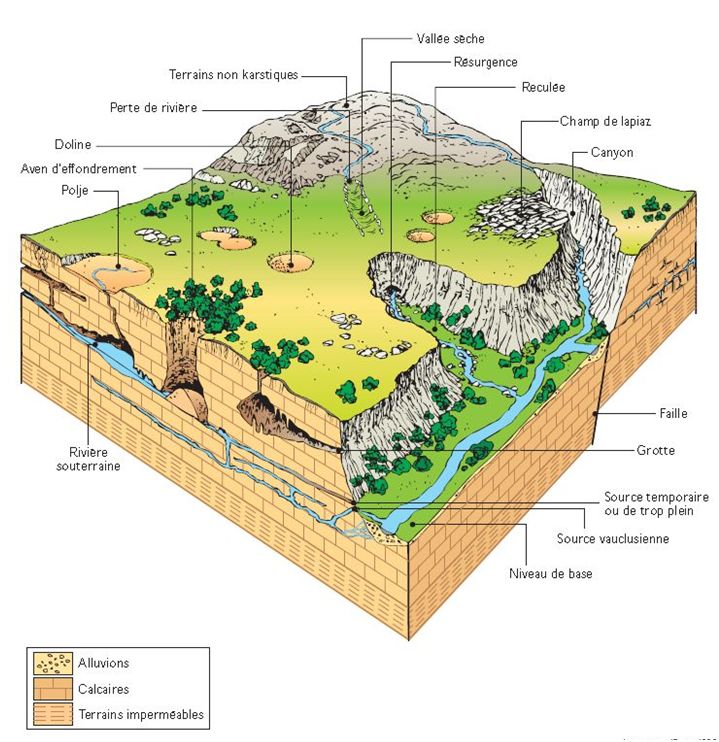
Source : Connaissance et gestion des ressources en eaux souterraines dans les régions karstiques, SDAGE Rhône-Méditerranée-Corse, 1999
Mécanisme de dissolution du calcaire par l’eau
Si la roche calcaire connait un processus d’érosion mécanique par le passage de l’eau, l’activité de dissolution de la roche est de loin bien plus importante.
L’eau de pluie se charge en dioxyde de carbone en traversant l’atmosphère. Elle poursuit ce chargement en traversant le sol où le CO2 est alors biogénique. L’eau devient de l’acide carbonique :
CO2 + H2O → H2CO3
Cet acide se dissocie en présence d’eau :
H2CO3 + H2O → HCO3– + H3O+
Le carbonate de calcium est alors attaqué par l’ion acide :
CaCO3 + H3O+ → Ca2+ + HCO3– + H2O (bicarbonate de calcium dissout)
L’ion carbonate Ca2+ passe en solution et est transporté par l’eau.
Les éléments non solubles sont laissés sur place, ce qui explique, dans les cavités, les épaisses couches d’argiles de décalcification, souvent ocres.

Grande draperie de concrétion dans une rivière souterraine du massif de la Sainte Baume (13)
Mécanisme du concrétionnement
Lorsque l’eau chargé d’ions Ca2+ débouche dans une cavité ou à l’air libre, c’est le phénomène inverse qui se produit : l’eau précipite du carbonate de calcium et forme des concrétions :
Ca2+ + 2HCO3– → CaCO3 + CO2 + H2O
C’est le départ de l’eau (évaporation) ou du dioxyde de carbone (dégazage) qui conduit à la précipitation du carbonate de calcium sous la forme d’aragonite ou de calcite.
| Si le dioxyde de carbone contribue à la dissolution et au transport du calcaire, dans l’eau des océans, ou des lacs, il est aussi à son origine : les océans captent le CO2 par dissolution au sein des eaux. Ce gaz, dissout, prend différentes formes appelées acide carbonique (H2CO3), hydrogénocarbonate (HCO3–) et carbonate (CO32-).Le CO2 de l’atmosphèrique peut donc se transformer en carbonate qui avec le calcium (Ca2+) dissout dans l’eau forme du CaCO3 :
CO32- + Ca2+ —> CaCO3 Ce carbonate de calcium est fixé par les coraux et mollusques pour former leurs carapaces, leurs coquilles ou leurs exostructures. A leur mort, celles-ci rejoindront le fond des mers, où pression et chaleur les transformeront en roche calcaire. |
En savoir plus
Bernard Collignon, Spéléologie, approches scientifique, 1988
